column
「獣医学つれづれ草」 第12話 抗菌薬の適応外使用から得た教訓 田村 豊 先生
抗菌薬の適応外使用から得た教訓
酪農学園大学名誉教授 田村 豊
動物で承認された抗菌薬は水産用を除いて要指示医薬品であるため、獣医師による投薬を基本としています。また食用になる家畜に対しての抗菌薬使用に当たっては、可食部位の残留を防止するため、「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律」(薬機法)に基づいて、「動物用医薬品及び医薬品の使用の規制に関する省令」(使用規制省令)に準拠した対象動物、用法及び用量、使用禁止期間を守ることが求められます。違反した場合は罰則の対象ともなっています。ただし、獣医師がその診療に係る対象動物の疾病の治療のため止むを得ないと判断した場合は、薬機法第八十三条の四の2により、獣医師自らが選定した抗菌薬で自ら決定した用法及び用量での投薬(適応外使用)が認められています。したがって、獣医師は自身の経験や知識をもとに、最良の獣医療を提供するために比較的自由に抗菌薬を使用することができるのです。ただし、当然のこととしてその責任も重く、適応外使用によって生じる安全性や残留性に関する責務は投薬した獣医師が一切を負うことになります。医療上重要な動物用第三世代セファロスポリン系薬であるセフチオフルナトリウム(CTF)を主成分とする製剤が承認されており、牛や豚の主に呼吸器感染症の治療に繁用されています。CTFは安全性と有効性に優れており、長期間にわたり畜産領域でも重要な抗菌薬として位置づけられています。今回はCTF製剤の肉用鶏への適応外使用により意図せぬ薬剤耐性菌の増加を招いた事例を紹介し、適応外使用に潜む問題点を考えてみたいと思います。
2018年の春、新聞に鶏肉の半数から医療で重要視されるESBL産生大腸菌が分離されるとのセンセーショナルなる記事が掲載され、消費者の関心を呼びました1)。ここでいうESBLですが基質特異性拡張型β‐ラクタマーゼという酵素で、ESBLを産生する細菌は医療で重篤な呼吸器系や尿路系細菌感染症で汎用されている全ての第三世代セファロスポリン系薬に耐性を示します。このことは加熱不十分の食肉を喫食することで、医療で重要な薬剤耐性菌が食肉からヒトへ伝播する可能性を示しています。この時、ESBL産生菌が原因とする感染症に罹患した患者は、治療にこの抗菌薬が使えないことを意味し、医療にとって重大な問題となるのです。今回の報道は、2015~2017年に集めた国産あるいは輸入の鶏肉を調べたところ、全体の49%からESBL産生菌を中心に薬剤耐性菌が分離されたという厚生労働省研究班での調査成績です2)。国産では59%、輸入で34%だったと述べています。文献でも国産鶏肉から41.3%、輸入鶏肉の53.3%からESBL産生大腸菌が分離されたとの報告があります3)。なお、ESBL産生大腸菌は、第三世代セファロスポリン系薬に耐性を示す大腸菌の中に含まれています。
ではこの時、肉用鶏から分離される大腸菌に対する第三世代セファロスポリン系薬の耐性率はどうだったのでしょうか?農林水産省の家畜衛生に関する薬剤耐性モニタリング体制(JVARM)の調査成績を見ると、第三世代セファロスポリン系薬であるセフォタキシム(CTX)の耐性率は2015年度で2.2%、2016年度で5.1%、2017年度で4.7%であり、この中の一部がESBL産生大腸菌ですのでさらに低い出現頻度となります4)。つまり、鶏肉から分離されたESBL産生大腸菌の由来を、肉用鶏が保有する大腸菌に直接的に結びつけるのには無理があるということです。
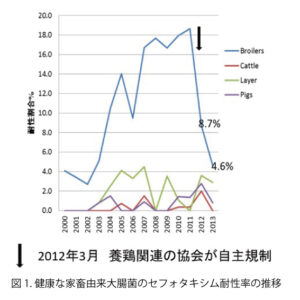
一方、2015年度以前の肉用鶏からのCTX耐性大腸菌の分離状況は、2015~2017年度の食肉から分離された大腸菌の状況とかなり異なっていました(図1)5)。つまり、2002年以降の健康な肉用鶏の糞便から分離された大腸菌に対するCTXの耐性率は急激に上昇し、20%近くまで達しています。この時、産卵鶏やウシやブタ由来大腸菌のCTX耐性率が5%以下であるのと対照的で明らかに異常です。この耐性率の上昇原因を調べたところ、鶏の胎児にCTFを適応外使用していることが明らかになったのです。鶏は様々な伝染病に罹る可能性があり、ワクチンプログラムが確立しています。しかし、多頭羽飼育が基本であることから、ワクチンの接種作業が非常に大きな労力を必要とします。そこで、鶏への効率的なワクチン接種を可能にしたものが自動卵内ワクチン接種システムです。卵内の鶏胎児にも成鶏に劣らぬ免疫応答力があるとの研究成果を基に、自動で卵内の胎児にワクチンを接種するもので、養鶏における革新的な技術といえるものです。しかし、卵表面は糞便由来細菌などで汚染しており、ワクチン接種時にしばしば胎児の細菌感染症を起こすことが問題視されていました。本来は卵表面を消毒するなど衛生管理を徹底すれば良いのですが、ワクチン液の中にCTFを混入し、安易な方法でヒナの細菌感染症を予防していたのです。つまり胎児の段階で高濃度の抗菌薬の投薬を受けていたことになり、ヒトや鶏以外の動物では到底想像もできないような話しです。2012年3月に事の重要性を認識した養鶏関連の協会が自主的にCTFの適応外使用を止めたところ、想像を遥かに超えて急激に耐性率は低下し、2013年には4.6%になっています。2014年度以降も2.2~5.1%で推移していることから、ほぼベースラインまで耐性率が低下していると思われます。4)。
今回の事例は私たちに抗菌薬の慎重使用の重要性を教えてくれているように感じます。効率性や利便性から抗菌薬を安易に適応外使用することにより、思いもしない急激な薬剤耐性菌の上昇を招いたことです。獣医師は抗菌薬の適応外使用が法的にも認められていますが、不適切な抗菌薬の使用が生み出す負の効果も考えて対処することが重要です。また、今回の事例はJVARMで毎年、同じ方法で試験をするというモニタリング制度の中で異常値が発見され、すぐに対処することで劇的に耐性率を低減化されたものであり、図らずもJVARMの有用性を示す結果となりました。実は肉用鶏由来大腸菌のCTX耐性率が急増する前の段階でも、JVARMの担当職員がESBL産生大腸菌を検出していました6)。当時、鶏用のセファロスポリン系薬が承認されておらず、また本剤は高価でしたので経済性からも鶏には使用しないだろうと考え、ESBL産生大腸菌がなぜ外見上健康な鶏の糞便から分離されたのか皆目見当がつきませんでした。分離された理由が不明であっても、CTX耐性率の異常値を検出する以前から、JVARMでは薬剤耐性菌の蔓延を予測したことになり、薬剤耐性菌対策として薬剤耐性菌の動向を把握することの重要性を示しています。
次に、鶏由来大腸菌のCTX耐性率が低いにも係わらず、鶏肉から分離される大腸菌の耐性率が高い理由を考えてみたいと思います。農場から小売店までの流れで薬剤耐性菌に汚染する過程を考えてみると、食肉加工工程に鍵があるように思われます。食肉加工工程で最も疑われるのは、内臓処理が行なわれた後の冷却水(チラー水)での浸漬工程です。内臓の摘出は自動でカッター処理をするのですが、この時、腸管を傷つけることがあります。もし、ESBL産生大腸菌を保有する鶏の腸管が傷つけられた場合、チラー水に薬剤耐性菌が拡散することになり、その後に浸漬された鶏肉の表面を汚染することが十分考えられます。実際には、チラー水に20ppmの次亜塩素酸ナトリウムが加えられており、細菌は死滅すると思われますが、糞便等の有機物の混入で、消毒効果が低下することが知られています。このようにして食肉の表面にESBL産生大腸菌が高頻度に汚染したのではないかと考えられます。
今回、抗菌薬の適応外使用から得た二つの教訓について紹介しました。繰り返しになりますが、感染症の治療にあたって獣医師による抗菌薬の慎重使用の励行が如何に重要であるかを示すとともに、JVARMの存在意義を示す結果になりました。なお、農林水産省では、「畜産物生産における動物用抗菌性物質製剤の慎重使用に関する基本的な考え方」7)を公表し、抗菌薬の慎重使用の普及・啓発活動を推進しています8)。
1)日本経済新聞:薬効かない菌、鶏肉の半数から検出 厚労省研究班.2018年3月31日薬効かない菌、鶏肉の半数から検出 厚労省研究班: 日本経済新聞 (nikkei.com)
2)渡邊治雄:食品由来薬剤耐性菌の発生動向及び衛生対策に関する研究.平成27~29年度 厚生労働科学研究費補助金総合報告書(H27-食品-一般-008),2018年3月.
3)山本詩織,朝倉宏,五十君静信:基質特異性拡張型βラクタマーゼ(ESBL)酸性菌に係わる最近の動向とその拡散に関する考察-食品汚染実態とその危害性について-.食衛誌 58(1):1-11, 2017.
4)農林水産省動物医薬品検査所:健康な家畜由来大腸菌の耐性率 https://www.maff.go.jp/nval/yakuzai/yakuzai_AMR_2.html
5)Hiki M, Kawanishi M, Abo H, Kojima A, Koike R, Hamamoto S, Asai T:Decreased resistance to broad-spectrum cephalosporin in Escherichia coli from healthy broilers at farms in Japan after voluntary withdrawal of ceftiofur. Foodborne Pathog Dis 12:639-643, 2015.
6)Kojima A, Ishii Y, Ishihara K, Esaki H, Asai T, Osa C, Tamura Y, Yamaguchi K: Extended-spectrum-β-lactamase-producingEscherichia coli strains isolated from farm animals from 1999 to 2002: Report from the Japanese veterinary antimicrobial resistance monitoring program. Antimicrob Agents Chemother 49:3533-3537,2005.
7)農林水産省:畜産物生産における動物用抗菌性物質製剤の慎重使用に関する基本的な考え方 https://www.maff.go.jp/j/syouan/tikusui/yakuzi/pdf/prudent_use.pdf
8)農林水産省:動物用抗菌剤の「責任ある慎重使用」を進めるために https://www.maff.go.jp/j/syouan/tikusui/yakuzi/pdf/vet_panf_prudent_use.pdf